QUÍMICA ANALÍTICA INSTRUMENTAL
Correlacione as colunas:
1 - Injetor ( ) Compõe a fase móvel na CG
2 - Gás de arraste ( ) promove a separação cromatográfica
3 - Manômetro ( ) vaporiza a amostra
4 - Coluna ( ) Promove o aquecimento do detector
5 - Forno ( ) Envia sinal elétrico para o amplificador
6 - Detector ( ) Controla a vazão do gás
A sequência que relaciona corretamente a coluna da esquerda com a coluna da direita é:
3 2 1 6 5 4
1 3 4 2 6 5
2 4 1 5 6 3
4 2 1 5 6 3
2 1 4 5 3 6
Na cromatografia gasosa, o tempo de retenção é determinado por alguns parâmetros. Para substâncias com peso molecular próximo, apresenta maior tempo de retenção aquela substância que:
Mais interage com a fase móvel.
Tem menor pressão de vapor.
Mais interage com a fase estacionária.
For mais polar.
Possuir menor densidade.
Em um laboratório, temos uma mistura contendo três substancias (A, B e C) cujas formulas estruturais estão representadas, a seguir. Empregando-se cromatografia de placa, tal mistura foi separada, e a placa obtida está colocada ao lado das estruturas. Sabendo-se que a fase móvel empregada foi o hexano, associa as manchas com as respectivas estruturas.
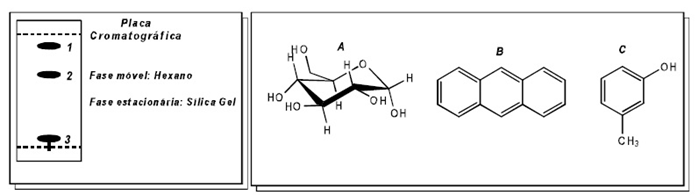
A 2; B 3; C 1.
A 3; B 2; C 1.
A 1; B 2; C 3.
A 3; B 1; C 2.
A 2; B 1; C 3.
Em uma análise cromatográfica de placa, na fase móvel as substâncias que queremos isolar são arrastadas por um solvente, que pode ser líquido ou gasoso. Imagine que você queira identificar um composto "polar", através dessa análise, qual dos compostos abaixo apresentaria maior polaridade, para atuar como fase móvel desse experimento?
Tetracloreto de metila
Alumina
Metanol
Hexano
Metano
Um químico realizando uma separação de dois compostos, usa uma fase estacionária polar e uma mistura (9:1) de dois solventes apolar e polar, respectivamente. No decorrer da separação ele percebe que a primeira substância saiu da coluna, porém a segunda ainda permanece próxima ao topo da coluna. Sugira ao químico como ele deverá proceder para conseguir a eluição da substância retida.
Trocando a fase estacionária normal por uma reversa.
Diminuindo a polaridade da fase estacionária.
Adicionando mais fase móvel a coluna.
Aumentando gradualmente a polaridade da fase móvel.
Aumentando bruscamente a polaridade da fase móvel.
Deseja-se separar uma mistura de octan-1-ol e octano. Para tal usa-se fase estacionária de sílica. Marque a alternativa que corresponde ao caráter predominante (polar ou apolar) da fase móvel para promover a separação e qual das duas substâncias sairá primeiro na coluna cromatográfica.
Apolar – Octan-1-ol
Polar – Octan-1-ol
Apolar – os dois compostos ficaram retidos
Polar – Octano
Apolar – Octano
Um determinado resíduo industrial, possui uma quantidade desconhecida de ACETATO DE CHUMBO Pb (C2H3O2)2. Uma amostra de 100 mL desse resíduo foi diluída em um balão de 1 L, do qual retirou-se certa quantidade para leitura em fotômetro de chama, apresentando a emissão no valor de 28,4 . Uma solução de Pb+2, com concentração de 4,27 x 10-4 mg/mL foi analisada e apresentou emissão de 12,7. Sabendo que a massa molar do acetato de chumbo é 325,29 g/mol e do íon Pb+2 é 209,98 g/mol, determine a concentração em g/L de Pb(C2H3O2)2 no resíduo industrial.
3,8 x 10-3 g/L de Pb(C2H3O2)2
1,34 x 10-2 g/L de Pb(C2H3O2)2
1,48 x 10-2 g/L de Pb(C2H3O2)2
6,11 x 10-6 g/L de Pb(C2H3O2)2
1,84 x 10-6 g/L de Pb(C2H3O2)2
Um processo na indústria farmacêutica, utiliza uma mistura de reagentes contendo cloreto de sódio (NaCl) em uma concentração determinada. Um técnico laboratorial recebeu uma amostra dessa mistura para confirmar a concentração e fez o seguinte teste: pesou 0,745 g da amostra e transferiu para um balão volumétrico de 250 mL. Retirou 5,00 mL dessa solução e transferiu para um balão de 50 mL e avolumou. A análise dessa solução apresentou emissão igual a 27. Determine a massa de Na+ em miligramas da amostra no balão de 250 mL, utilizando a curva analítica de calibração mostrada abaixo.
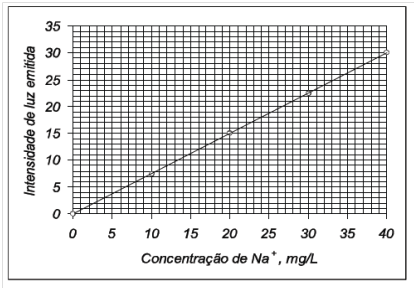
165 mg de Na+ no balão de 250 mL
115 mg de Na+ no balão de 250 mL
30 mg de Na+ no balão de 250 mL
62 mg de Na+ no balão de 250 mL
90 mg de Na+ no balão de 250 mL
O controle de qualidade da matéria-prima é de grande importância na indústria química sendo que este pode ser utilizado para qualificar fornecedores. Suponha que você esteja em seu laboratório e tenha recebido lotes de um dado polímero do fornecedor A e do fornecedor B. No intuito de se verificar o teor de polímero nos dois lotes recebidos você preparou uma curva de calibração representada a seguir:
Abs = 0,0579 C 0,001 (mg/L); R2 = 0,9999.
Posteriormente você pesou uma amostra de 0,300 g do produto recebido de cada fornecedor. A seguir dissolveu-se cada uma das massas separadamente, transferindo-as para dois balões volumétricos de 500,0 mL, tendo o seu volume completado até a marca. A partir das duas soluções preparadas anteriormente, foram transferidos 1,00 mL de cada uma delas para balões volumétricos de 100,0 mL, tendo o seu volume completado até a marca. Ao se realizar as medidas de absorbância o valor encontrado para solução do polímero (amostra) obtida a partir do fornecedor A foi de 0,328 enquanto que aquela preparada do polímero (amostra) do fornecedor B foi de 0,346. Com base nessas informações pede-se: Calcular o teor (%) de polímero encontrado na matéria-prima de cada um dos fornecedores, respectivamente. (A e B).
94,67% e 99,83%
99,83% e 94,67%
54,55% e 44,65%
50,00% e 90,00%
49,76% e 83,99%
Para determinar o mercúrio (Hg) contido em uma amostra de água contaminada, utilizou-se a curva analítica Abs = 0,0603 CHg2+ + 0,0079, onde a concentração de mercúrio é dada em mg/L. A amostra de água apresentou uma absorbância de 0,522. Qual a concentração de mercúrio na amostra?
1 - Injetor ( ) Compõe a fase móvel na CG
A sequência que relaciona corretamente a coluna da esquerda com a coluna da direita é:
3 2 1 6 5 4
1 3 4 2 6 5
2 4 1 5 6 3
4 2 1 5 6 3
2 1 4 5 3 6
Na cromatografia gasosa, o tempo de retenção é determinado por alguns parâmetros. Para substâncias com peso molecular próximo, apresenta maior tempo de retenção aquela substância que:
Mais interage com a fase móvel.
Tem menor pressão de vapor.
Mais interage com a fase estacionária.
For mais polar.
Possuir menor densidade.
Em um laboratório, temos uma mistura contendo três substancias (A, B e C) cujas formulas estruturais estão representadas, a seguir. Empregando-se cromatografia de placa, tal mistura foi separada, e a placa obtida está colocada ao lado das estruturas. Sabendo-se que a fase móvel empregada foi o hexano, associa as manchas com as respectivas estruturas.

A 2; B 3; C 1.
A 3; B 2; C 1.
A 1; B 2; C 3.
A 3; B 1; C 2.
A 2; B 1; C 3.
Em uma análise cromatográfica de placa, na fase móvel as substâncias que queremos isolar são arrastadas por um solvente, que pode ser líquido ou gasoso. Imagine que você queira identificar um composto "polar", através dessa análise, qual dos compostos abaixo apresentaria maior polaridade, para atuar como fase móvel desse experimento?
Tetracloreto de metila
Alumina
Metanol
Hexano
Metano
Um químico realizando uma separação de dois compostos, usa uma fase estacionária polar e uma mistura (9:1) de dois solventes apolar e polar, respectivamente. No decorrer da separação ele percebe que a primeira substância saiu da coluna, porém a segunda ainda permanece próxima ao topo da coluna. Sugira ao químico como ele deverá proceder para conseguir a eluição da substância retida.
Trocando a fase estacionária normal por uma reversa.
Diminuindo a polaridade da fase estacionária.
Adicionando mais fase móvel a coluna.
Aumentando gradualmente a polaridade da fase móvel.
Aumentando bruscamente a polaridade da fase móvel.
Deseja-se separar uma mistura de octan-1-ol e octano. Para tal usa-se fase estacionária de sílica. Marque a alternativa que corresponde ao caráter predominante (polar ou apolar) da fase móvel para promover a separação e qual das duas substâncias sairá primeiro na coluna cromatográfica.
Apolar – Octan-1-ol
Polar – Octan-1-ol
Apolar – os dois compostos ficaram retidos
Polar – Octano
Apolar – Octano
Um determinado resíduo industrial, possui uma quantidade desconhecida de ACETATO DE CHUMBO Pb (C2H3O2)2. Uma amostra de 100 mL desse resíduo foi diluída em um balão de 1 L, do qual retirou-se certa quantidade para leitura em fotômetro de chama, apresentando a emissão no valor de 28,4 . Uma solução de Pb+2, com concentração de 4,27 x 10-4 mg/mL foi analisada e apresentou emissão de 12,7. Sabendo que a massa molar do acetato de chumbo é 325,29 g/mol e do íon Pb+2 é 209,98 g/mol, determine a concentração em g/L de Pb(C2H3O2)2 no resíduo industrial.
3,8 x 10-3 g/L de Pb(C2H3O2)2
1,34 x 10-2 g/L de Pb(C2H3O2)2
1,48 x 10-2 g/L de Pb(C2H3O2)2
6,11 x 10-6 g/L de Pb(C2H3O2)2
1,84 x 10-6 g/L de Pb(C2H3O2)2
Um processo na indústria farmacêutica, utiliza uma mistura de reagentes contendo cloreto de sódio (NaCl) em uma concentração determinada. Um técnico laboratorial recebeu uma amostra dessa mistura para confirmar a concentração e fez o seguinte teste: pesou 0,745 g da amostra e transferiu para um balão volumétrico de 250 mL. Retirou 5,00 mL dessa solução e transferiu para um balão de 50 mL e avolumou. A análise dessa solução apresentou emissão igual a 27. Determine a massa de Na+ em miligramas da amostra no balão de 250 mL, utilizando a curva analítica de calibração mostrada abaixo.

165 mg de Na+ no balão de 250 mL
115 mg de Na+ no balão de 250 mL
30 mg de Na+ no balão de 250 mL
62 mg de Na+ no balão de 250 mL
90 mg de Na+ no balão de 250 mL
O controle de qualidade da matéria-prima é de grande importância na indústria química sendo que este pode ser utilizado para qualificar fornecedores. Suponha que você esteja em seu laboratório e tenha recebido lotes de um dado polímero do fornecedor A e do fornecedor B. No intuito de se verificar o teor de polímero nos dois lotes recebidos você preparou uma curva de calibração representada a seguir:
Abs = 0,0579 C 0,001 (mg/L); R2 = 0,9999.
Posteriormente você pesou uma amostra de 0,300 g do produto recebido de cada fornecedor. A seguir dissolveu-se cada uma das massas separadamente, transferindo-as para dois balões volumétricos de 500,0 mL, tendo o seu volume completado até a marca. A partir das duas soluções preparadas anteriormente, foram transferidos 1,00 mL de cada uma delas para balões volumétricos de 100,0 mL, tendo o seu volume completado até a marca. Ao se realizar as medidas de absorbância o valor encontrado para solução do polímero (amostra) obtida a partir do fornecedor A foi de 0,328 enquanto que aquela preparada do polímero (amostra) do fornecedor B foi de 0,346. Com base nessas informações pede-se: Calcular o teor (%) de polímero encontrado na matéria-prima de cada um dos fornecedores, respectivamente. (A e B).
94,67% e 99,83%
99,83% e 94,67%
54,55% e 44,65%
50,00% e 90,00%
49,76% e 83,99%
Para determinar o mercúrio (Hg) contido em uma amostra de água contaminada, utilizou-se a curva analítica Abs = 0,0603 CHg2+ + 0,0079, onde a concentração de mercúrio é dada em mg/L. A amostra de água apresentou uma absorbância de 0,522. Qual a concentração de mercúrio na amostra?
Mais interage com a fase móvel.
Tem menor pressão de vapor.
Mais interage com a fase estacionária.
For mais polar.
Possuir menor densidade.
Em um laboratório, temos uma mistura contendo três substancias (A, B e C) cujas formulas estruturais estão representadas, a seguir. Empregando-se cromatografia de placa, tal mistura foi separada, e a placa obtida está colocada ao lado das estruturas. Sabendo-se que a fase móvel empregada foi o hexano, associa as manchas com as respectivas estruturas.

A 2; B 3; C 1.
A 3; B 2; C 1.
A 1; B 2; C 3.
A 3; B 1; C 2.
A 2; B 1; C 3.
Em uma análise cromatográfica de placa, na fase móvel as substâncias que queremos isolar são arrastadas por um solvente, que pode ser líquido ou gasoso. Imagine que você queira identificar um composto "polar", através dessa análise, qual dos compostos abaixo apresentaria maior polaridade, para atuar como fase móvel desse experimento?
Tetracloreto de metila
Alumina
Metanol
Hexano
Metano
Um químico realizando uma separação de dois compostos, usa uma fase estacionária polar e uma mistura (9:1) de dois solventes apolar e polar, respectivamente. No decorrer da separação ele percebe que a primeira substância saiu da coluna, porém a segunda ainda permanece próxima ao topo da coluna. Sugira ao químico como ele deverá proceder para conseguir a eluição da substância retida.
Trocando a fase estacionária normal por uma reversa.
Diminuindo a polaridade da fase estacionária.
Adicionando mais fase móvel a coluna.
Aumentando gradualmente a polaridade da fase móvel.
Aumentando bruscamente a polaridade da fase móvel.
Deseja-se separar uma mistura de octan-1-ol e octano. Para tal usa-se fase estacionária de sílica. Marque a alternativa que corresponde ao caráter predominante (polar ou apolar) da fase móvel para promover a separação e qual das duas substâncias sairá primeiro na coluna cromatográfica.
Apolar – Octan-1-ol
Polar – Octan-1-ol
Apolar – os dois compostos ficaram retidos
Polar – Octano
Apolar – Octano
Um determinado resíduo industrial, possui uma quantidade desconhecida de ACETATO DE CHUMBO Pb (C2H3O2)2. Uma amostra de 100 mL desse resíduo foi diluída em um balão de 1 L, do qual retirou-se certa quantidade para leitura em fotômetro de chama, apresentando a emissão no valor de 28,4 . Uma solução de Pb+2, com concentração de 4,27 x 10-4 mg/mL foi analisada e apresentou emissão de 12,7. Sabendo que a massa molar do acetato de chumbo é 325,29 g/mol e do íon Pb+2 é 209,98 g/mol, determine a concentração em g/L de Pb(C2H3O2)2 no resíduo industrial.
3,8 x 10-3 g/L de Pb(C2H3O2)2
1,34 x 10-2 g/L de Pb(C2H3O2)2
1,48 x 10-2 g/L de Pb(C2H3O2)2
6,11 x 10-6 g/L de Pb(C2H3O2)2
1,84 x 10-6 g/L de Pb(C2H3O2)2
Um processo na indústria farmacêutica, utiliza uma mistura de reagentes contendo cloreto de sódio (NaCl) em uma concentração determinada. Um técnico laboratorial recebeu uma amostra dessa mistura para confirmar a concentração e fez o seguinte teste: pesou 0,745 g da amostra e transferiu para um balão volumétrico de 250 mL. Retirou 5,00 mL dessa solução e transferiu para um balão de 50 mL e avolumou. A análise dessa solução apresentou emissão igual a 27. Determine a massa de Na+ em miligramas da amostra no balão de 250 mL, utilizando a curva analítica de calibração mostrada abaixo.

165 mg de Na+ no balão de 250 mL
115 mg de Na+ no balão de 250 mL
30 mg de Na+ no balão de 250 mL
62 mg de Na+ no balão de 250 mL
90 mg de Na+ no balão de 250 mL
O controle de qualidade da matéria-prima é de grande importância na indústria química sendo que este pode ser utilizado para qualificar fornecedores. Suponha que você esteja em seu laboratório e tenha recebido lotes de um dado polímero do fornecedor A e do fornecedor B. No intuito de se verificar o teor de polímero nos dois lotes recebidos você preparou uma curva de calibração representada a seguir:
Abs = 0,0579 C 0,001 (mg/L); R2 = 0,9999.
Posteriormente você pesou uma amostra de 0,300 g do produto recebido de cada fornecedor. A seguir dissolveu-se cada uma das massas separadamente, transferindo-as para dois balões volumétricos de 500,0 mL, tendo o seu volume completado até a marca. A partir das duas soluções preparadas anteriormente, foram transferidos 1,00 mL de cada uma delas para balões volumétricos de 100,0 mL, tendo o seu volume completado até a marca. Ao se realizar as medidas de absorbância o valor encontrado para solução do polímero (amostra) obtida a partir do fornecedor A foi de 0,328 enquanto que aquela preparada do polímero (amostra) do fornecedor B foi de 0,346. Com base nessas informações pede-se: Calcular o teor (%) de polímero encontrado na matéria-prima de cada um dos fornecedores, respectivamente. (A e B).
94,67% e 99,83%
99,83% e 94,67%
54,55% e 44,65%
50,00% e 90,00%
49,76% e 83,99%
Para determinar o mercúrio (Hg) contido em uma amostra de água contaminada, utilizou-se a curva analítica Abs = 0,0603 CHg2+ + 0,0079, onde a concentração de mercúrio é dada em mg/L. A amostra de água apresentou uma absorbância de 0,522. Qual a concentração de mercúrio na amostra?

A 2; B 3; C 1.
A 3; B 2; C 1.
A 1; B 2; C 3.
A 3; B 1; C 2.
A 2; B 1; C 3.
Em uma análise cromatográfica de placa, na fase móvel as substâncias que queremos isolar são arrastadas por um solvente, que pode ser líquido ou gasoso. Imagine que você queira identificar um composto "polar", através dessa análise, qual dos compostos abaixo apresentaria maior polaridade, para atuar como fase móvel desse experimento?
Tetracloreto de metila
Alumina
Metanol
Hexano
Metano
Um químico realizando uma separação de dois compostos, usa uma fase estacionária polar e uma mistura (9:1) de dois solventes apolar e polar, respectivamente. No decorrer da separação ele percebe que a primeira substância saiu da coluna, porém a segunda ainda permanece próxima ao topo da coluna. Sugira ao químico como ele deverá proceder para conseguir a eluição da substância retida.
Trocando a fase estacionária normal por uma reversa.
Diminuindo a polaridade da fase estacionária.
Adicionando mais fase móvel a coluna.
Aumentando gradualmente a polaridade da fase móvel.
Aumentando bruscamente a polaridade da fase móvel.
Deseja-se separar uma mistura de octan-1-ol e octano. Para tal usa-se fase estacionária de sílica. Marque a alternativa que corresponde ao caráter predominante (polar ou apolar) da fase móvel para promover a separação e qual das duas substâncias sairá primeiro na coluna cromatográfica.
Apolar – Octan-1-ol
Polar – Octan-1-ol
Apolar – os dois compostos ficaram retidos
Polar – Octano
Apolar – Octano
Um determinado resíduo industrial, possui uma quantidade desconhecida de ACETATO DE CHUMBO Pb (C2H3O2)2. Uma amostra de 100 mL desse resíduo foi diluída em um balão de 1 L, do qual retirou-se certa quantidade para leitura em fotômetro de chama, apresentando a emissão no valor de 28,4 . Uma solução de Pb+2, com concentração de 4,27 x 10-4 mg/mL foi analisada e apresentou emissão de 12,7. Sabendo que a massa molar do acetato de chumbo é 325,29 g/mol e do íon Pb+2 é 209,98 g/mol, determine a concentração em g/L de Pb(C2H3O2)2 no resíduo industrial.
3,8 x 10-3 g/L de Pb(C2H3O2)2
1,34 x 10-2 g/L de Pb(C2H3O2)2
1,48 x 10-2 g/L de Pb(C2H3O2)2
6,11 x 10-6 g/L de Pb(C2H3O2)2
1,84 x 10-6 g/L de Pb(C2H3O2)2
Um processo na indústria farmacêutica, utiliza uma mistura de reagentes contendo cloreto de sódio (NaCl) em uma concentração determinada. Um técnico laboratorial recebeu uma amostra dessa mistura para confirmar a concentração e fez o seguinte teste: pesou 0,745 g da amostra e transferiu para um balão volumétrico de 250 mL. Retirou 5,00 mL dessa solução e transferiu para um balão de 50 mL e avolumou. A análise dessa solução apresentou emissão igual a 27. Determine a massa de Na+ em miligramas da amostra no balão de 250 mL, utilizando a curva analítica de calibração mostrada abaixo.

165 mg de Na+ no balão de 250 mL
115 mg de Na+ no balão de 250 mL
30 mg de Na+ no balão de 250 mL
62 mg de Na+ no balão de 250 mL
90 mg de Na+ no balão de 250 mL
O controle de qualidade da matéria-prima é de grande importância na indústria química sendo que este pode ser utilizado para qualificar fornecedores. Suponha que você esteja em seu laboratório e tenha recebido lotes de um dado polímero do fornecedor A e do fornecedor B. No intuito de se verificar o teor de polímero nos dois lotes recebidos você preparou uma curva de calibração representada a seguir:
Abs = 0,0579 C 0,001 (mg/L); R2 = 0,9999.
Posteriormente você pesou uma amostra de 0,300 g do produto recebido de cada fornecedor. A seguir dissolveu-se cada uma das massas separadamente, transferindo-as para dois balões volumétricos de 500,0 mL, tendo o seu volume completado até a marca. A partir das duas soluções preparadas anteriormente, foram transferidos 1,00 mL de cada uma delas para balões volumétricos de 100,0 mL, tendo o seu volume completado até a marca. Ao se realizar as medidas de absorbância o valor encontrado para solução do polímero (amostra) obtida a partir do fornecedor A foi de 0,328 enquanto que aquela preparada do polímero (amostra) do fornecedor B foi de 0,346. Com base nessas informações pede-se: Calcular o teor (%) de polímero encontrado na matéria-prima de cada um dos fornecedores, respectivamente. (A e B).
94,67% e 99,83%
99,83% e 94,67%
54,55% e 44,65%
50,00% e 90,00%
49,76% e 83,99%
Para determinar o mercúrio (Hg) contido em uma amostra de água contaminada, utilizou-se a curva analítica Abs = 0,0603 CHg2+ + 0,0079, onde a concentração de mercúrio é dada em mg/L. A amostra de água apresentou uma absorbância de 0,522. Qual a concentração de mercúrio na amostra?
Tetracloreto de metila
Alumina
Metanol
Hexano
Metano
Um químico realizando uma separação de dois compostos, usa uma fase estacionária polar e uma mistura (9:1) de dois solventes apolar e polar, respectivamente. No decorrer da separação ele percebe que a primeira substância saiu da coluna, porém a segunda ainda permanece próxima ao topo da coluna. Sugira ao químico como ele deverá proceder para conseguir a eluição da substância retida.
Trocando a fase estacionária normal por uma reversa.
Diminuindo a polaridade da fase estacionária.
Adicionando mais fase móvel a coluna.
Aumentando gradualmente a polaridade da fase móvel.
Aumentando bruscamente a polaridade da fase móvel.
Deseja-se separar uma mistura de octan-1-ol e octano. Para tal usa-se fase estacionária de sílica. Marque a alternativa que corresponde ao caráter predominante (polar ou apolar) da fase móvel para promover a separação e qual das duas substâncias sairá primeiro na coluna cromatográfica.
Apolar – Octan-1-ol
Polar – Octan-1-ol
Apolar – os dois compostos ficaram retidos
Polar – Octano
Apolar – Octano
Um determinado resíduo industrial, possui uma quantidade desconhecida de ACETATO DE CHUMBO Pb (C2H3O2)2. Uma amostra de 100 mL desse resíduo foi diluída em um balão de 1 L, do qual retirou-se certa quantidade para leitura em fotômetro de chama, apresentando a emissão no valor de 28,4 . Uma solução de Pb+2, com concentração de 4,27 x 10-4 mg/mL foi analisada e apresentou emissão de 12,7. Sabendo que a massa molar do acetato de chumbo é 325,29 g/mol e do íon Pb+2 é 209,98 g/mol, determine a concentração em g/L de Pb(C2H3O2)2 no resíduo industrial.
3,8 x 10-3 g/L de Pb(C2H3O2)2
1,34 x 10-2 g/L de Pb(C2H3O2)2
1,48 x 10-2 g/L de Pb(C2H3O2)2
6,11 x 10-6 g/L de Pb(C2H3O2)2
1,84 x 10-6 g/L de Pb(C2H3O2)2
Um processo na indústria farmacêutica, utiliza uma mistura de reagentes contendo cloreto de sódio (NaCl) em uma concentração determinada. Um técnico laboratorial recebeu uma amostra dessa mistura para confirmar a concentração e fez o seguinte teste: pesou 0,745 g da amostra e transferiu para um balão volumétrico de 250 mL. Retirou 5,00 mL dessa solução e transferiu para um balão de 50 mL e avolumou. A análise dessa solução apresentou emissão igual a 27. Determine a massa de Na+ em miligramas da amostra no balão de 250 mL, utilizando a curva analítica de calibração mostrada abaixo.

165 mg de Na+ no balão de 250 mL
115 mg de Na+ no balão de 250 mL
30 mg de Na+ no balão de 250 mL
62 mg de Na+ no balão de 250 mL
90 mg de Na+ no balão de 250 mL
O controle de qualidade da matéria-prima é de grande importância na indústria química sendo que este pode ser utilizado para qualificar fornecedores. Suponha que você esteja em seu laboratório e tenha recebido lotes de um dado polímero do fornecedor A e do fornecedor B. No intuito de se verificar o teor de polímero nos dois lotes recebidos você preparou uma curva de calibração representada a seguir:
Abs = 0,0579 C 0,001 (mg/L); R2 = 0,9999.
Posteriormente você pesou uma amostra de 0,300 g do produto recebido de cada fornecedor. A seguir dissolveu-se cada uma das massas separadamente, transferindo-as para dois balões volumétricos de 500,0 mL, tendo o seu volume completado até a marca. A partir das duas soluções preparadas anteriormente, foram transferidos 1,00 mL de cada uma delas para balões volumétricos de 100,0 mL, tendo o seu volume completado até a marca. Ao se realizar as medidas de absorbância o valor encontrado para solução do polímero (amostra) obtida a partir do fornecedor A foi de 0,328 enquanto que aquela preparada do polímero (amostra) do fornecedor B foi de 0,346. Com base nessas informações pede-se: Calcular o teor (%) de polímero encontrado na matéria-prima de cada um dos fornecedores, respectivamente. (A e B).
94,67% e 99,83%
99,83% e 94,67%
54,55% e 44,65%
50,00% e 90,00%
49,76% e 83,99%
Para determinar o mercúrio (Hg) contido em uma amostra de água contaminada, utilizou-se a curva analítica Abs = 0,0603 CHg2+ + 0,0079, onde a concentração de mercúrio é dada em mg/L. A amostra de água apresentou uma absorbância de 0,522. Qual a concentração de mercúrio na amostra?
Trocando a fase estacionária normal por uma reversa.
Diminuindo a polaridade da fase estacionária.
Adicionando mais fase móvel a coluna.
Aumentando gradualmente a polaridade da fase móvel.
Aumentando bruscamente a polaridade da fase móvel.
Deseja-se separar uma mistura de octan-1-ol e octano. Para tal usa-se fase estacionária de sílica. Marque a alternativa que corresponde ao caráter predominante (polar ou apolar) da fase móvel para promover a separação e qual das duas substâncias sairá primeiro na coluna cromatográfica.
Apolar – Octan-1-ol
Polar – Octan-1-ol
Apolar – os dois compostos ficaram retidos
Polar – Octano
Apolar – Octano
Um determinado resíduo industrial, possui uma quantidade desconhecida de ACETATO DE CHUMBO Pb (C2H3O2)2. Uma amostra de 100 mL desse resíduo foi diluída em um balão de 1 L, do qual retirou-se certa quantidade para leitura em fotômetro de chama, apresentando a emissão no valor de 28,4 . Uma solução de Pb+2, com concentração de 4,27 x 10-4 mg/mL foi analisada e apresentou emissão de 12,7. Sabendo que a massa molar do acetato de chumbo é 325,29 g/mol e do íon Pb+2 é 209,98 g/mol, determine a concentração em g/L de Pb(C2H3O2)2 no resíduo industrial.
3,8 x 10-3 g/L de Pb(C2H3O2)2
1,34 x 10-2 g/L de Pb(C2H3O2)2
1,48 x 10-2 g/L de Pb(C2H3O2)2
6,11 x 10-6 g/L de Pb(C2H3O2)2
1,84 x 10-6 g/L de Pb(C2H3O2)2
Um processo na indústria farmacêutica, utiliza uma mistura de reagentes contendo cloreto de sódio (NaCl) em uma concentração determinada. Um técnico laboratorial recebeu uma amostra dessa mistura para confirmar a concentração e fez o seguinte teste: pesou 0,745 g da amostra e transferiu para um balão volumétrico de 250 mL. Retirou 5,00 mL dessa solução e transferiu para um balão de 50 mL e avolumou. A análise dessa solução apresentou emissão igual a 27. Determine a massa de Na+ em miligramas da amostra no balão de 250 mL, utilizando a curva analítica de calibração mostrada abaixo.

165 mg de Na+ no balão de 250 mL
115 mg de Na+ no balão de 250 mL
30 mg de Na+ no balão de 250 mL
62 mg de Na+ no balão de 250 mL
90 mg de Na+ no balão de 250 mL
O controle de qualidade da matéria-prima é de grande importância na indústria química sendo que este pode ser utilizado para qualificar fornecedores. Suponha que você esteja em seu laboratório e tenha recebido lotes de um dado polímero do fornecedor A e do fornecedor B. No intuito de se verificar o teor de polímero nos dois lotes recebidos você preparou uma curva de calibração representada a seguir:
Abs = 0,0579 C 0,001 (mg/L); R2 = 0,9999.
Posteriormente você pesou uma amostra de 0,300 g do produto recebido de cada fornecedor. A seguir dissolveu-se cada uma das massas separadamente, transferindo-as para dois balões volumétricos de 500,0 mL, tendo o seu volume completado até a marca. A partir das duas soluções preparadas anteriormente, foram transferidos 1,00 mL de cada uma delas para balões volumétricos de 100,0 mL, tendo o seu volume completado até a marca. Ao se realizar as medidas de absorbância o valor encontrado para solução do polímero (amostra) obtida a partir do fornecedor A foi de 0,328 enquanto que aquela preparada do polímero (amostra) do fornecedor B foi de 0,346. Com base nessas informações pede-se: Calcular o teor (%) de polímero encontrado na matéria-prima de cada um dos fornecedores, respectivamente. (A e B).
94,67% e 99,83%
99,83% e 94,67%
54,55% e 44,65%
50,00% e 90,00%
49,76% e 83,99%
Para determinar o mercúrio (Hg) contido em uma amostra de água contaminada, utilizou-se a curva analítica Abs = 0,0603 CHg2+ + 0,0079, onde a concentração de mercúrio é dada em mg/L. A amostra de água apresentou uma absorbância de 0,522. Qual a concentração de mercúrio na amostra?
Apolar – Octan-1-ol
Polar – Octan-1-ol
Apolar – os dois compostos ficaram retidos
Polar – Octano
Apolar – Octano
Um determinado resíduo industrial, possui uma quantidade desconhecida de ACETATO DE CHUMBO Pb (C2H3O2)2. Uma amostra de 100 mL desse resíduo foi diluída em um balão de 1 L, do qual retirou-se certa quantidade para leitura em fotômetro de chama, apresentando a emissão no valor de 28,4 . Uma solução de Pb+2, com concentração de 4,27 x 10-4 mg/mL foi analisada e apresentou emissão de 12,7. Sabendo que a massa molar do acetato de chumbo é 325,29 g/mol e do íon Pb+2 é 209,98 g/mol, determine a concentração em g/L de Pb(C2H3O2)2 no resíduo industrial.
3,8 x 10-3 g/L de Pb(C2H3O2)2
1,34 x 10-2 g/L de Pb(C2H3O2)2
1,48 x 10-2 g/L de Pb(C2H3O2)2
6,11 x 10-6 g/L de Pb(C2H3O2)2
1,84 x 10-6 g/L de Pb(C2H3O2)2
Um processo na indústria farmacêutica, utiliza uma mistura de reagentes contendo cloreto de sódio (NaCl) em uma concentração determinada. Um técnico laboratorial recebeu uma amostra dessa mistura para confirmar a concentração e fez o seguinte teste: pesou 0,745 g da amostra e transferiu para um balão volumétrico de 250 mL. Retirou 5,00 mL dessa solução e transferiu para um balão de 50 mL e avolumou. A análise dessa solução apresentou emissão igual a 27. Determine a massa de Na+ em miligramas da amostra no balão de 250 mL, utilizando a curva analítica de calibração mostrada abaixo.

165 mg de Na+ no balão de 250 mL
115 mg de Na+ no balão de 250 mL
30 mg de Na+ no balão de 250 mL
62 mg de Na+ no balão de 250 mL
90 mg de Na+ no balão de 250 mL
O controle de qualidade da matéria-prima é de grande importância na indústria química sendo que este pode ser utilizado para qualificar fornecedores. Suponha que você esteja em seu laboratório e tenha recebido lotes de um dado polímero do fornecedor A e do fornecedor B. No intuito de se verificar o teor de polímero nos dois lotes recebidos você preparou uma curva de calibração representada a seguir:
Abs = 0,0579 C 0,001 (mg/L); R2 = 0,9999.
Posteriormente você pesou uma amostra de 0,300 g do produto recebido de cada fornecedor. A seguir dissolveu-se cada uma das massas separadamente, transferindo-as para dois balões volumétricos de 500,0 mL, tendo o seu volume completado até a marca. A partir das duas soluções preparadas anteriormente, foram transferidos 1,00 mL de cada uma delas para balões volumétricos de 100,0 mL, tendo o seu volume completado até a marca. Ao se realizar as medidas de absorbância o valor encontrado para solução do polímero (amostra) obtida a partir do fornecedor A foi de 0,328 enquanto que aquela preparada do polímero (amostra) do fornecedor B foi de 0,346. Com base nessas informações pede-se: Calcular o teor (%) de polímero encontrado na matéria-prima de cada um dos fornecedores, respectivamente. (A e B).
94,67% e 99,83%
99,83% e 94,67%
54,55% e 44,65%
50,00% e 90,00%
49,76% e 83,99%
Para determinar o mercúrio (Hg) contido em uma amostra de água contaminada, utilizou-se a curva analítica Abs = 0,0603 CHg2+ + 0,0079, onde a concentração de mercúrio é dada em mg/L. A amostra de água apresentou uma absorbância de 0,522. Qual a concentração de mercúrio na amostra?
3,8 x 10-3 g/L de Pb(C2H3O2)2
1,34 x 10-2 g/L de Pb(C2H3O2)2
1,48 x 10-2 g/L de Pb(C2H3O2)2
6,11 x 10-6 g/L de Pb(C2H3O2)2
1,84 x 10-6 g/L de Pb(C2H3O2)2
Um processo na indústria farmacêutica, utiliza uma mistura de reagentes contendo cloreto de sódio (NaCl) em uma concentração determinada. Um técnico laboratorial recebeu uma amostra dessa mistura para confirmar a concentração e fez o seguinte teste: pesou 0,745 g da amostra e transferiu para um balão volumétrico de 250 mL. Retirou 5,00 mL dessa solução e transferiu para um balão de 50 mL e avolumou. A análise dessa solução apresentou emissão igual a 27. Determine a massa de Na+ em miligramas da amostra no balão de 250 mL, utilizando a curva analítica de calibração mostrada abaixo.

165 mg de Na+ no balão de 250 mL
115 mg de Na+ no balão de 250 mL
30 mg de Na+ no balão de 250 mL
62 mg de Na+ no balão de 250 mL
90 mg de Na+ no balão de 250 mL
O controle de qualidade da matéria-prima é de grande importância na indústria química sendo que este pode ser utilizado para qualificar fornecedores. Suponha que você esteja em seu laboratório e tenha recebido lotes de um dado polímero do fornecedor A e do fornecedor B. No intuito de se verificar o teor de polímero nos dois lotes recebidos você preparou uma curva de calibração representada a seguir:
Abs = 0,0579 C 0,001 (mg/L); R2 = 0,9999.
Posteriormente você pesou uma amostra de 0,300 g do produto recebido de cada fornecedor. A seguir dissolveu-se cada uma das massas separadamente, transferindo-as para dois balões volumétricos de 500,0 mL, tendo o seu volume completado até a marca. A partir das duas soluções preparadas anteriormente, foram transferidos 1,00 mL de cada uma delas para balões volumétricos de 100,0 mL, tendo o seu volume completado até a marca. Ao se realizar as medidas de absorbância o valor encontrado para solução do polímero (amostra) obtida a partir do fornecedor A foi de 0,328 enquanto que aquela preparada do polímero (amostra) do fornecedor B foi de 0,346. Com base nessas informações pede-se: Calcular o teor (%) de polímero encontrado na matéria-prima de cada um dos fornecedores, respectivamente. (A e B).
94,67% e 99,83%
99,83% e 94,67%
54,55% e 44,65%
50,00% e 90,00%
49,76% e 83,99%
Para determinar o mercúrio (Hg) contido em uma amostra de água contaminada, utilizou-se a curva analítica Abs = 0,0603 CHg2+ + 0,0079, onde a concentração de mercúrio é dada em mg/L. A amostra de água apresentou uma absorbância de 0,522. Qual a concentração de mercúrio na amostra?

165 mg de Na+ no balão de 250 mL
115 mg de Na+ no balão de 250 mL
30 mg de Na+ no balão de 250 mL
62 mg de Na+ no balão de 250 mL
90 mg de Na+ no balão de 250 mL
O controle de qualidade da matéria-prima é de grande importância na indústria química sendo que este pode ser utilizado para qualificar fornecedores. Suponha que você esteja em seu laboratório e tenha recebido lotes de um dado polímero do fornecedor A e do fornecedor B. No intuito de se verificar o teor de polímero nos dois lotes recebidos você preparou uma curva de calibração representada a seguir:
Abs = 0,0579 C 0,001 (mg/L); R2 = 0,9999.
Posteriormente você pesou uma amostra de 0,300 g do produto recebido de cada fornecedor. A seguir dissolveu-se cada uma das massas separadamente, transferindo-as para dois balões volumétricos de 500,0 mL, tendo o seu volume completado até a marca. A partir das duas soluções preparadas anteriormente, foram transferidos 1,00 mL de cada uma delas para balões volumétricos de 100,0 mL, tendo o seu volume completado até a marca. Ao se realizar as medidas de absorbância o valor encontrado para solução do polímero (amostra) obtida a partir do fornecedor A foi de 0,328 enquanto que aquela preparada do polímero (amostra) do fornecedor B foi de 0,346. Com base nessas informações pede-se: Calcular o teor (%) de polímero encontrado na matéria-prima de cada um dos fornecedores, respectivamente. (A e B).
94,67% e 99,83%
99,83% e 94,67%
54,55% e 44,65%
50,00% e 90,00%
49,76% e 83,99%
Para determinar o mercúrio (Hg) contido em uma amostra de água contaminada, utilizou-se a curva analítica Abs = 0,0603 CHg2+ + 0,0079, onde a concentração de mercúrio é dada em mg/L. A amostra de água apresentou uma absorbância de 0,522. Qual a concentração de mercúrio na amostra?
94,67% e 99,83%
99,83% e 94,67%
54,55% e 44,65%
50,00% e 90,00%
49,76% e 83,99%